
- DAZ.online
- News
- Apotheke
- Erstmals Xarelto-Generika...
Trotz Patent-Streit
Erstmals Xarelto-Generika im Handel
Stuttgart - 18.04.2024, 14:45 Uhr

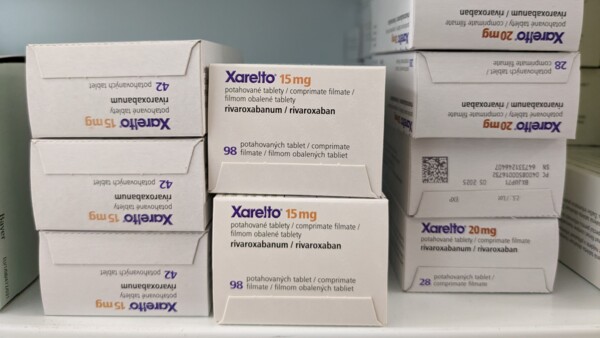
Xarelto gibt es in verschiedenen Dosierungen, doch nur eine davon ist in Deutschland jetzt auch als Generikum erhältlich. (Foto: Semi / AdobeStock)
Seit dem 15. April sind erstmals Rivaroxaban-Generika in der Lauer-Taxe gelistet. Der eine oder die andere Apotheken-Mitarbeiter:in dürfte dabei über die Tatsache stolpern, dass diese – anders als das Original Xarelto – nur in der 2,5-mg-Dosierung verfügbar sind. Dahinter verbirgt sich ein komplizierter Patent-Streit.
Am 2. April ist Bayers Xarelto®-Patent ausgelaufen. Damit sind seit dem 15. April in der Lauer-Taxe® Rivaroxaban-Generika wie
- Nabaxor (Biocon Pharma Malta I Ltd.),
- Rivarolto (TAD Pharma GmbH), oder
- Rivaxa (Glenmark Arzneimittel GmbH) gelistet.
Die meisten neuen Generika tragen den Wirkstoffnamen im Handelsnamen und stammen beispielsweise von Zentiva, Viatris, Stada, Ratiopharm, Betapharm, Aliud, Accord Healthcare, Abdi Farma, 1A Pharma oder der 089PHARM GmbH.
Alle Generika sind allerdings nur in der 2,5-mg-Dosierung verfügbar.
Dosierungspatent gilt noch bis Januar 2026 – oder doch nicht?
Wie die Online-Plattform „Juve Patent“ am 2. April informierte, liegt das daran, dass lediglich das Basis-Patent für den Wirkstoff Rivaroxaban abgelaufen ist. Bayer habe weiterhin ein Dosierungspatent auf die einmal tägliche Einnahme inne, das noch bis Januar 2026 gilt – solange Patentgerichte nicht anders entscheiden, hieß es. Doch kann eine einmal tägliche Einnahme als patentierungswürdige Erfindung eingestuft werden?
Tatsächlich sei das Patent bereits widerrufen gewesen, ehe die Beschwerdekammer des Europäischen Patentamts das Patent 2021 wieder in Kraft setzte. Nun sei der Streit kürzlich neu aufgeflammt: Gerichte in München und Den Haag hätten der Sicht von Bayer recht gegeben. Doch beispielsweise in Paris wurde der französische Teil des Patents jetzt offenbar für ungültig erklärt. Wie die Nachrichtenagentur Reuters am 12. April berichtete, hat auch ein britisches Gericht mittlerweile das Dosispatent für ungültig erklärt. Grund sei, dass bei der Entwicklung des Arzneimittels keine „erfinderische Tätigkeit“ vorliege.
Mehr zum Thema

Bayer bricht Studie ab
Asundexian – Gerinnungshemmer mit geringerem Blutungsrisiko enttäuscht

Bayer-Blockbuster
Wettbewerber greifen Xarelto-Patent an
In den Wirtschaftsmedien werden schon lange die Auswirkungen des Patentauslaufs von Xarelto® für Bayer diskutiert. Hoffnung auf einen weiteren Blockbuster hatte der Gerinnungshemmer Asundexian gemacht. Doch Bayer musste vergangenes Jahr eine Phase-III-Studie aufgrund mangelnder Wirkung abbrechen. Das erklärt wohl unter anderem, warum Bayer so hartnäckig an seinem Xarelto®-Dosis-Patent festhält.
























0 Kommentare
Kommentar abgeben